Estados da Matéria: Uma Exploração: Exemplo De Matéria No Estado Sólido Líquido E Gasoso Atividades
Exemplo De Matéria No Estado Sólido Líquido E Gasoso Atividades – A matéria, tudo que ocupa espaço e possui massa, existe em diferentes estados físicos, principalmente sólido, líquido e gasoso. Compreender as características desses estados é fundamental para entender o mundo ao nosso redor, desde a formação das rochas até o funcionamento de nossos aparelhos eletrônicos. A diferença entre esses estados reside na organização das partículas (átomos e moléculas) e na energia cinética dessas partículas.
Estados da Matéria: Sólido, Líquido e Gasoso

Os estados sólido, líquido e gasoso são definidos pela força de atração entre as partículas constituintes e pela sua energia cinética. Nos sólidos, as partículas estão fortemente ligadas, com baixa energia cinética, resultando em uma forma e volume definidos. Nos líquidos, as partículas têm maior energia cinética e estão menos ligadas, o que permite que eles assumam a forma do recipiente, mas mantenham um volume constante.
Já nos gases, as partículas possuem alta energia cinética e forças de atração muito fracas, podendo se expandir para ocupar todo o volume disponível.
| Propriedade | Sólido | Líquido | Gasoso |
|---|---|---|---|
| Forma | Definitiva | Indefinida (assume a forma do recipiente) | Indefinida (ocupa todo o volume disponível) |
| Volume | Definitivo | Definitivo | Indefinido (expansível) |
| Compressibilidade | Baixa | Baixa | Alta |
| Energia Cinética | Baixa | Média | Alta |
| Organização Molecular | Alta organização, partículas próximas e ordenadas | Organização intermediária, partículas próximas mas menos ordenadas | Baixa organização, partículas distantes e desordenada |
Exemplos de Materiais em Cada Estado Físico
A observação de materiais em diferentes estados físicos é crucial para a compreensão das propriedades da matéria. A seguir, apresentamos exemplos de materiais encontrados naturalmente em cada um dos estados, com suas propriedades físicas e químicas relevantes.
- Sólido: Gelo (H₂O), Diamante (C), Ferro (Fe), Granito (silicatos), Sal de cozinha (NaCl). Suas propriedades incluem alta densidade, forma definida e baixa compressibilidade. O gelo, por exemplo, apresenta uma estrutura cristalina ordenada, enquanto o diamante é conhecido por sua dureza excepcional devido às fortes ligações covalentes entre átomos de carbono.
- Líquido: Água (H₂O), Álcool (C₂H₅OH), Mercúrio (Hg), Óleo vegetal, Leite. Apresentam volume definido, mas forma indefinida, adaptando-se à forma do recipiente. A água, por exemplo, é um solvente universal, capaz de dissolver uma grande variedade de substâncias.
- Gasoso: Oxigênio (O₂), Nitrogênio (N₂), Dióxido de carbono (CO₂), Hélio (He), Vapor d’água (H₂O). Caracterizados por alta compressibilidade e ausência de forma e volume definidos. O oxigênio, essencial para a respiração, é um gás incolor e inodoro.
Mudanças de Estado Físico, Exemplo De Matéria No Estado Sólido Líquido E Gasoso Atividades
As mudanças de estado físico são processos que envolvem a transição da matéria de um estado para outro, devido à variação de temperatura e/ou pressão. Esses processos são reversíveis e envolvem trocas de energia.
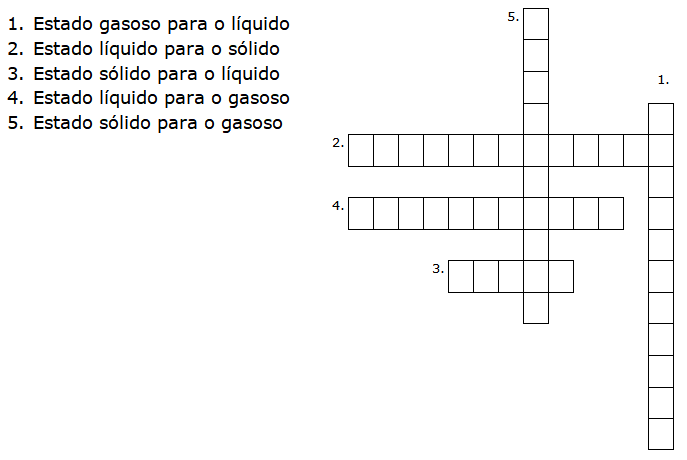
A fusão é a passagem do estado sólido para o líquido; a solidificação é o processo inverso. A vaporização é a transformação do líquido em gás; a condensação é a transformação do gás em líquido. A sublimação é a passagem direta do sólido para o gasoso; e a deposição é a transformação do gasoso para o sólido, sem passar pelo estado líquido.
Um diagrama representando essas mudanças poderia ser visualizado como um hexágono. Cada vértice representaria um estado físico (sólido, líquido, gasoso). As arestas que conectam os vértices representariam as mudanças de estado (fusão, solidificação, vaporização, condensação, sublimação, deposição). As setas indicariam a direção da mudança e o sentido do fluxo de energia (absorção ou liberação de calor). Por exemplo, a seta da fusão apontaria do sólido para o líquido, indicando absorção de calor.
Atividades Práticas: Observando Mudanças de Estado
Experimentos práticos auxiliam na compreensão das mudanças de estado da matéria. As atividades a seguir propõem observações diretas desses processos.
- Fusão do Gelo: Materiais: Cubos de gelo, copo, termômetro. Procedimento: Coloque os cubos de gelo em um copo e monitore a temperatura enquanto o gelo derrete. Resultados Esperados: O gelo derreterá à medida que a temperatura aumentar, passando do estado sólido para o líquido. Conclusão: A fusão é um processo endotérmico (absorve calor).
- Evaporação da Água: Materiais: Água, panela, fogão. Procedimento: Aqueça a água em uma panela até a ebulição. Observe o que acontece. Resultados Esperados: A água evaporará, passando do estado líquido para o gasoso. Conclusão: A vaporização é um processo endotérmico (absorve calor).
- Condensação do Vapor: Materiais: Água fervente, recipiente de vidro frio. Procedimento: Coloque o recipiente de vidro frio acima da água fervente. Observe a superfície do vidro. Resultados Esperados: Gotículas de água se formarão na superfície do vidro. Conclusão: O vapor d’água se condensa ao entrar em contato com uma superfície fria, passando do estado gasoso para o líquido.
Aplicações dos Estados da Matéria no Cotidiano
Os diferentes estados da matéria desempenham papéis cruciais em diversas aplicações do nosso dia a dia. As propriedades de cada estado são exploradas para diferentes finalidades.
- Refrigeração: A mudança de estado da água (líquido para sólido) é utilizada na refrigeração de alimentos. O gelo absorve calor do ambiente, mantendo os alimentos frescos.
- Produção de Energia: A vaporização da água é utilizada em usinas termoelétricas para gerar energia. O vapor de alta pressão move turbinas que geram eletricidade.
- Construção Civil: O estado sólido de materiais como concreto e aço é essencial para a construção de edifícios e infraestruturas. A resistência e a rigidez desses materiais são fundamentais para a estabilidade das construções.
Modelos Atômicos e Estados Físicos da Matéria

Os modelos atômicos evoluíram ao longo do tempo, fornecendo diferentes perspectivas sobre a estrutura da matéria e sua relação com os estados físicos. O modelo de Dalton propunha átomos indivisíveis e esferas maciças, enquanto o modelo de Thomson introduziu a ideia de elétrons embebidos em uma esfera de carga positiva (pudim de passas). O modelo de Rutherford, por sua vez, descreveu o átomo com um núcleo denso e positivo cercado por elétrons em órbita.
As forças intermoleculares, como as forças de van der Waals e as ligações de hidrogênio, influenciam diretamente os estados físicos da matéria. Forças intermoleculares fortes levam a estados sólidos com pontos de fusão e ebulição altos, enquanto forças fracas resultam em líquidos ou gases com pontos de fusão e ebulição baixos. A intensidade dessas forças varia com a estrutura molecular e a polaridade das moléculas, influenciando diretamente o arranjo e a mobilidade das partículas, determinando, assim, o estado físico da matéria.
Concluímos nossa exploração dos estados da matéria, compreendendo a intrincada relação entre organização molecular, energia cinética e as propriedades macroscópicas que observamos diariamente. De atividades práticas que revelam as mudanças de estado a aplicações cotidianas que dependem dessas transformações, a viagem pelo mundo microscópico nos forneceu uma perspectiva mais ampla e integrada da ciência. As diferenças entre sólido, líquido e gasoso, inicialmente percebidas como simples, revelam uma complexidade fascinante, evidenciando a importância de investigar e entender os princípios fundamentais da natureza.
Esperamos que esta jornada tenha estimulado a curiosidade e o desejo de explorar ainda mais os mistérios da matéria e seus infinitos estados.

